Kiderült, hogy a gorilláknak köszönhetjük a gyilkos maláriát


A Wellcome Trust Sanger Institute (WTSI, Egyesült Királyság) és a Montpellier-i Egyetem (Franciaország) kutatói elsőként követték vissza azokat a genetikai eseményeket, amelyek révén a legveszedelmesebb malária-parazita átkerülhetett a gorillákról az emberekre.
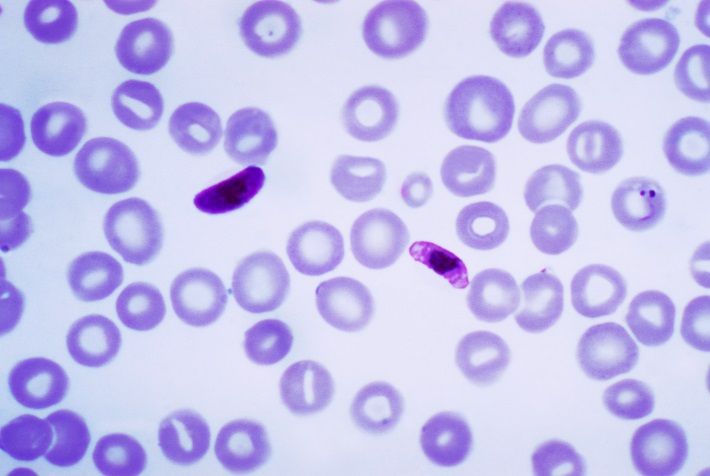
Nagyjából 50 ezer évvel ezelőtt tűnhetett fel először az a génszekvencia a Plasmodium falciparum genomjában, amely képessé tette a kórokozót az emberi vörösvérsejtek fertőzésére.

Az eredmények azt mutatják, hogy az rh5 gén korlátozott ideig lehetővé tette a parazita számára mind az emberi, mint a gorilla gazdaszervezetek megtámadását, ami molekuláris szinten magyarázatot ad a fajok közötti ugrás megtörténtére.
A csoport azt a DNS-mutációt is azonosította, amely később az emberekre korlátozta a P. falciparum terjedését,
ezzel lezárva az ideiglenes fajközi átjárót.
A PLOS Biology legfrissebb számában közölt tanulmány nemcsak feltárja annak történetét, hogyan hódította meg az emberiséget a világ azóta is legpusztítóbb fertőző betegsége, hanem általában útmutatást ad a kórokozók fajok közötti ugrásainak jobb megértéséhez.
A malária, noha ezt a mi mérsékelt égövi lakóhelyünkön (egyelőre) nem érzékeljük, a mai napig az emberiséget érő egyik legnagyobb egészségügyi fenyegetés, amely becslések szerint 435 ezer életet olt ki évente.
Az áldozatok 61 százaléka ráadásul az 5 évesnél fiatalabb gyerekek közül kerül ki.
Bár maláriát a Plasmodium rokoni körének több faja okozhat, a betegség leginkább halálos formájáért a P. falciparum felelős. Ez a faj különösen az afrikai kontinensen elterjedt, ahol 2017-ben a maláriás megbetegedések 99,7 százalékát okozta.
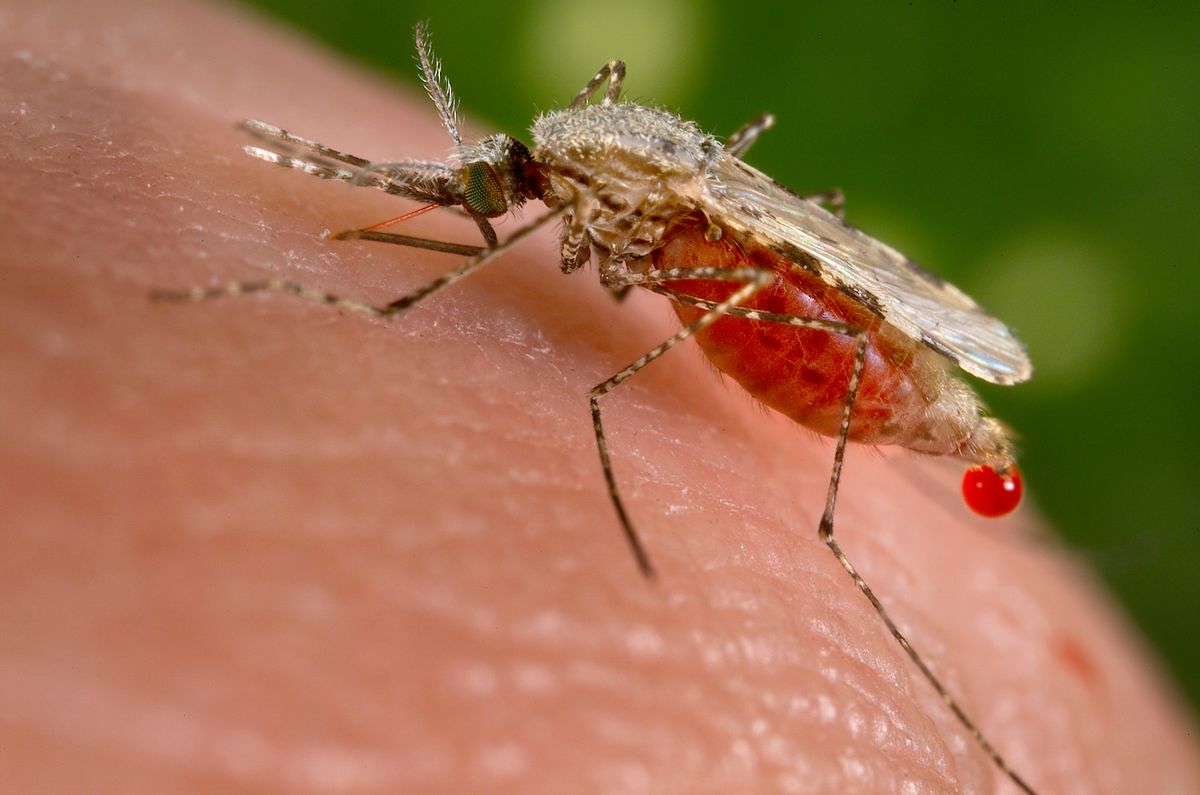
A Laverania családba tartozó parazitáknak hét faja okoz maláriaszerű megbetegedést.
Valamennyien az afrikai emberszabásúak kórokozójaként kezdték pályafutásukat,
és ma mindegyikük egyetlen gazdafajra korlátozódik: három maláriaparazitájuk van a csimpánzoknak és három a gorilláknak.
A hetedik, a P. falciparum ma már kizárólag embereket fertőz, az után, hogy nagyjából 50 ezer évvel ezelőtt a zoonózis nevű folyamat révén átugrott a gorillagazdákról az emberekre.

Mikor megszekvenálták a Laverania család mind a hét maláriaokozó parazitafajának genomját, napvilágra került annak a DNS-szakasznak a szekvenciája is, amelyet a P. falciparum őse a gorilla-parazitától a Plasmodium adleri-től örökölt.
Ezen a DNS-szakaszon belül azonosították az RH5 nevű gént,
amely az emberi vörösvérsejtek felszínéhez való kötődésben kulcsszerepet játszó RH5 fehérjét kódolja.
Az RH5 fehérje receptora az emberi vörösvérsejteken a basigin nevű fehérje, és kettejük kölcsönhatása kritikus a P. falciparum fertőzőképessége szempontjából.
Éppen ezért az RH5-basigin kölcsönhatás ígéretes célpontja lehet egy majdani maláriaoltásnak,
mert ha ezt a kapcsolatot megakadályozzuk, a parazita képtelen belépni az emberi vörösvérsejtekbe és betegséget okozni.
A P. falciparum eredetének pontos tisztázása végett a Montpellier-i Egyetem kutatói visszakövetkeztették, mi lehetett az az eredeti RH5 DNS-szekvencia, amelyet a P. falciparum őse 50 ezer éve a P. adleri-től átvett.
A „feltámasztott" ősi RH5 gén szintetikus másolatait a WTSI munkatársai készítették el, és ugyanitt lehetőség nyílt a rekonstruált RH5 fehérje molekuláris kölcsönhatásainak vizsgálatára is.

A kutatók arra számítottak, hogy a P. adleri által a P. falciparum ősének átadott RH5 fehérje csak a gorilla vörösvérsejtjeinek basigin receptorához tud majd kötődni,
de nagy meglepetésükre a fehérje a gorilláé mellett az emberi basiginnel is kölcsönhatást tudott létesíteni.
Innen azonnal adta magát az ötlet, hogy miként történhetett a fajok közötti átkapcsolás.
„A tény, hogy az ősi RH5 fehérje az emberi és a gorilla basigin receptorhoz egyaránt képes volt kötődni, közvetlenül kínálta annak a molekuláris szintű magyarázatát, hogyan evolvált a P. falciparum az emberi fertőzőképesség irányába" – összegezte Francis Galaway, a WTSI tudományos munkatársa és a cikk írója.
A következőkben Galaway és kollégái hat különbséget azonosítottak
az ősi és a P. falciparum mai RH5-szekvenciája között.

E mutációk egyike a gorilla basigin receptorához való kötődés képességének teljes elvesztését okozta, ami pedig azt világítja meg, hogy a fajközi ugrás után miként vált a P. falciparum kizárólagosan emberi parazitává.
„Lenyűgöző, hogy képesek vagyunk 'újraéleszteni' egy rég letűnt gént, ez esetben azt, amely lehetővé tette a Plasmodium falciparum számára a gorilla mellett az emberi gazdaszervezetek fertőzését – mondta Franck Prugnolle a Montpellier-i Egyetemről.

– Nemcsak azt fedeztük fel, miként történt a gazdafajváltás, de még azt a konkrét mutációt is megtaláltuk, amely aztán a P. falciparumot végérvényesen egy gazdafajhoz, az emberhez láncolta."
Zoonózisról akkor beszélünk, ha egy betegség – például az influenza vagy a malária – állatokról emberre ugrik át.
Ehhez az szükséges, hogy az állati gazdát fertőző kórokozó olyan genetikai anyagra tegyen szert, amely lehetséges gazdáinak körét kiterjeszti az emberre.
A P. falciparum okozta malária esetében az RH5 gén transzfere a feltételezések szerint úgy mehetett végbe, hogy a gorilla sejtjeibe egyszerre két Plasmodium faj egyedei férkőztek.

Az ilyen, introgressziónak nevezett folyamat során
a két faj genetikai anyagot tud cserélni egymással.
Az a fajta introgressziós esemény, amely a P. falciparum gorilláról emberre ugrását előkészíthette, hihetetlenül ritka: a teljes Laverania család hét fajának összehasonlító genomi elemzése során több millió éves időskálán mindössze néhány ilyen géncsere nyomaira bukkantak.
„Nem kérdés, hogy az emberiség történetében a Plasmodium falciparum több halálesetért tehető felelőssé, mint bármely más kórokozó – szögezte le Gavin Wright, a WTSI csoportvezetője és a közlemény vezető szerzője. – Ezért egyszerre fontos és magával ragadó felderíteni azokat a molekuláris útvonalakat, amelyek megnyitották e gyilkos kórokozó előtt az emberi fertőzés kapuját."












