Szenzációs felfedezés: itt az új szer, ami hatásos a rák ellen

Bár az oltás révén a legtöbben életmentő védettséget szerezhetnek a COVID-19-cel szemben, a tudósok továbbra is keresik a súlyos lefolyású fertőzések kezelésének módjait. Nemcsak azért, mert akadnak, akik orvosi okból nem kaphatnak oltást, hanem azért is, mert felbukkanhatnak a vírusnak olyan új, veszélyes törzsei,
amelyek ellen a vakcina csak részleges védelmet nyújt.
Most a Dél-Kaliforniai Egyetem (University of Southern California, USC) orvosi fakultásán, a Keck School of Medicine-en dolgozó kutatók a biokémiát és molekuláris medicínát oktató Amy S. Lee professzor vezetésével arról jelentettek meg közleményt a Nature Communications szakfolyóiratban, hogy a GRP78 néven ismert ún. chaperonfehérje, amely ismerten szerepet játszik más vírusok szaporodásában, a SARS-CoV-2 másolódásához is elengedhetetlen.
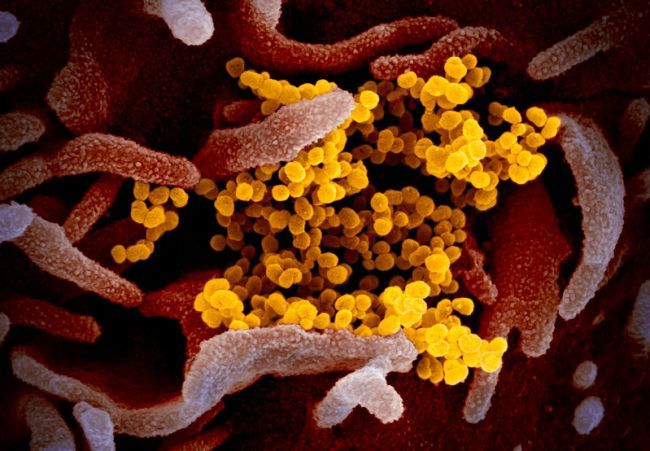
A tanulmányban megmutatják, hogy a GRP78 termelésének leállításával vagy aktivitásának gátlásával
nagy mértékben visszaszorítható a SARS-CoV-2 replikációja.
A szerzők szerint a szer újfajta védelmet kínál a COVID-19-cel szemben, méghozzá olyat, amely az esetleges jövőbeni törzsekkel szemben ugyanúgy működőképes marad.
„A SARS-CoV-2 elleni küzdelemben az egyik legnagyobb probléma az, hogy a vírus folyamatosan mutál, s így oly módon adaptálódik, hogy egyre hatékonyabbá váljék a gazdasejt fertőzése és a benne történő sokszorozódás terén – magyarázza Lee. – Ha tehát a vírust kergetjük, ez nehéz ügy lesz, és a kimenetel megjósolhatatlan."
A Keck School of Medicine és a Cleveland Clinic Florida Research and Innovation Center kutatói ezért stabilabb eszközöket szerettek volna fejleszteni a COVID-19 elleni harc céljaira.
Így kezdtek bele a GRP78 nevű kulcsfontosságú chaperonfehérje – más fehérjék működőképessége fölött őrködő molekuláris „gardedám" – funkciójának vizsgálatába. A chaperonfehérjék, köztük a GRP78, a többi fehérjének segítenek abban, hogy felvegyék a működésükhöz szükséges térbeli alakzatot.
Míg az egészséges sejtek viszonylag kevés GRP78-cal is jól elműködnek, a stresszhatás alatt álló sejteknek jóval több GRP78-ra van szükségük ahhoz, hogy a nehézségekkel megbirkózzanak.
A Keck School of Medicine csapata egy 2021-es cikkben már megmutatta, hogy amikor a SARS-CoV-2 megjelenik a színen, túszul ejti a GRP78-at, és arra kényszeríti, hogy más fogadófehérjékkel (receptorokkal) együttműködve elősegítse a vírus bejutását a sejtbe.
A sejt belsejében aztán a vírus szaporodik, és onnan kijutva tovaterjed a szervezetben. Az azonban mindeddig nem volt világos, vajon a GRP78 „szükséges és elengedhetetlen"-e ahhoz, hogy a SARS-CoV-2 az emberi tüdőhámsejtekben szaporodjék.
SARS-CoV-2-vel fertőzött emberi tüdőhámsejteket vizsgálva a csoport megállapította, hogy a fertőzés intenzitásának növekedtével a sejtek egyre több GRP78-at termelnek.
Lee és munkatársai ezután egy hírvivő RNS-alapú speciális eszköz segítségével gátolták a sejttenyészetben fenntartott emberi tüdőhámsejtek GRP78-termelését anélkül, hogy egyéb sejtszintű folyamatokba beavatkoztak volna.
Amikor ezeket a sejteket utóbb SARS-CoV-2-vel fertőzték, a sejtek kevesebb virális tüskefehérjét termeltek,
és jóval kevesebb olyan vírusrészecskét bocsátottak ki, amely továbbvihette volna a fertőzést. Ezzel bizonyították, hogy a GRP78 nemcsak szükséges, de nélkülözhetetlen is a vírus szaporodásához és az új vírusrészecskék összeszereléséhez.
„Immár közvetlen bizonyítékunk van arra, hogy a GRP78 egy vírust támogató fehérje, amely elengedhetetlen a SARS-CoV-2 replikációjához" – erősíti meg Lee. A tudósok tovább vizsgálódtak, hogy megbizonyosodjanak felőle, csakugyan megfékezhető-e a COVID-19 a GRP78 gátlásán keresztül.
Teszteltek hát egy HA15 néven futó, frissen azonosított kismolekulájú gyógyszert, amelyet eredetileg daganatok kezelésére fejlesztettek ki azzal az elgondolással, hogy a rákos sejtekben fajlagosan hozzákötődik majd a GRP78-hoz és gátolja annak tevékenységét.
„És láss csodát, azt találtuk, hogy a szer rendkívül hatékonyan csökkentette a SARS-CoV-2 által keltett plakkok méretét és számát olyan biztonságos dózisban adva, amely az ép sejteket nem károsítja"– nyilatkozta Lee.
A plakkok azok a kerekded tarfoltok, amelyek egy sejttenyészetben keletkeznek vírusfertőzés és az azt követő tömeges sejtelhalás nyomán.
A kutatók ezt követően olyan genetikailag módosított egereken próbálták ki a HA15-öt, amelyek emberi SARS-CoV-2-receptorokat fejeznek ki a tüdőhámsejtjeiken. Amikor ezeket az egereket SARS-CoV-2-vel fertőzték, a HA15 nagy mértékben csökkentette a tüdők vírusterhelését.
Ezzel párhuzamosan Lee és munkatársai a Michigani Egyetem kutatóival együttműködve a HA15, valamint egy másik GRP78-gátlószer, a YUM70 daganatellenes hatékonyságát is vizsgálják. Felfedezték, hogy mindkét GRP78-gátló, a HA15 és a YUM70 is visszaszorítja a mutáns KRAS onkogén fehérje termelődését,
s ezáltal csökkenti a KRAS-mutációt hordozó hasnyálmirigy-, tüdő- és vastagbélrák-sejttenyészetek életképességét.
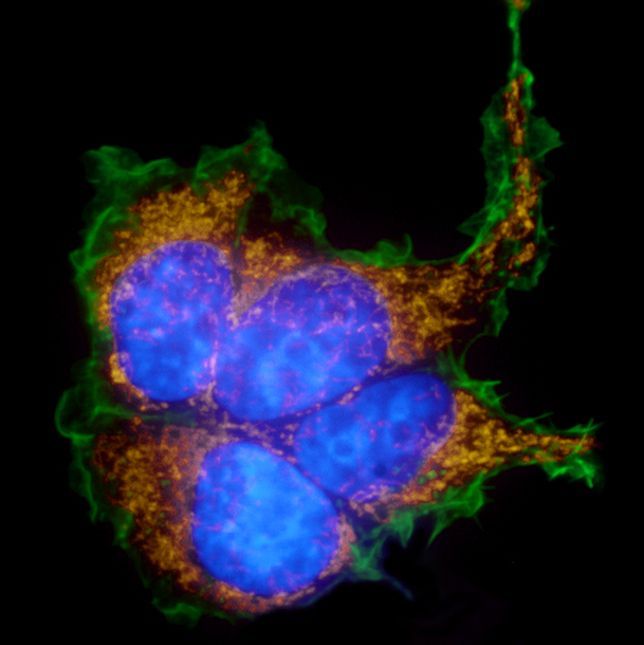
A KRAS sejtszaporodást szabályozó fehérje mutációi gyakoriak a daganatokban, és a mutáns KRAS-t eddig gyógyszerekkel kiüthetetlen célpontnak tartották. Ezeket az eredményeket, amelyek szerint a GRP78 támadása segítheti e halálos daganatok leküzdését, a Neoplasia című onkológiai folyóiratban hozták nyilvánosságra.
Egyelőre mindkét cikk csak ún. proof of principle-típusú, vagyis egy elv érvényességét igazoló tanulmány.
A HA15 és YUM70 biztonságosságának és hatékonyságának alátámasztásához még sok további kutatásra,
legfőképpen emberi klinikai vizsgálatokra lesz majd szükség.
De ezeket a vegyületek más GRP78 inhibitorok mellett már tesztelik lehetséges COVID-19-ellenes és daganatellenes terápiaként egyaránt. A GRP78-at gátló gyógyszerek családja bármely olyan, a jövőben esetleg megjelenő koronavírussal szemben is hatékony lehet, amelynek a sejtbe való belépését és szaporodását szintén elősegíti a GRP78.












