Így kell megakadályozni a dobozos italok kispriccelését nyitáskor


A szénsavas dobozos ital kinyitásakor hallható szisszenést a folyadékból megszökő gázbuborékok adják. A gáz felszabadulásának oka, hogy megváltozik az italban lévő szén-dioxid (CO2) oldhatósága. A zárt dobozban lévő nagyjából 3 bar nyomás nyitáskor lecsökken a levegő 1 bar atmoszférikus nyomására.
A gázok oldhatósága pedig a nyomás csökkenésével csökken. Míg 3 bar nyomáson 4,5 gramm CO2 oldódik egy liter vízben, addig 1 baron csak körülbelül 1,5 gramm.
A doboz kinyitása előtt mikroszkopikus gázbuborékok tapadnak a doboz belsejéhez. A doboz kinyitásakor e buborékoknak megnő a mérete, a CO2 oldhatóságának csökkenése miatt. Amikor a buborékok elérnek egy bizonyos méretet, leválnak a falról és felemelkednek a folyadék tetejére, miközben kiszorítják az útjukba eső folyadékot.
De milyen szerepet játszhat a doboz tetejének ütögetése a folyamatban? A The Conversation magazin ismertet egy elméletet arról, hogy miért lehet hatékony ez a módszer a kihabzás elkerülésére.
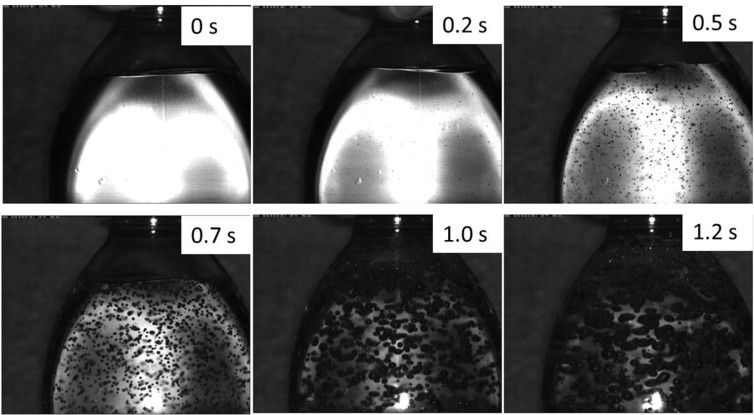
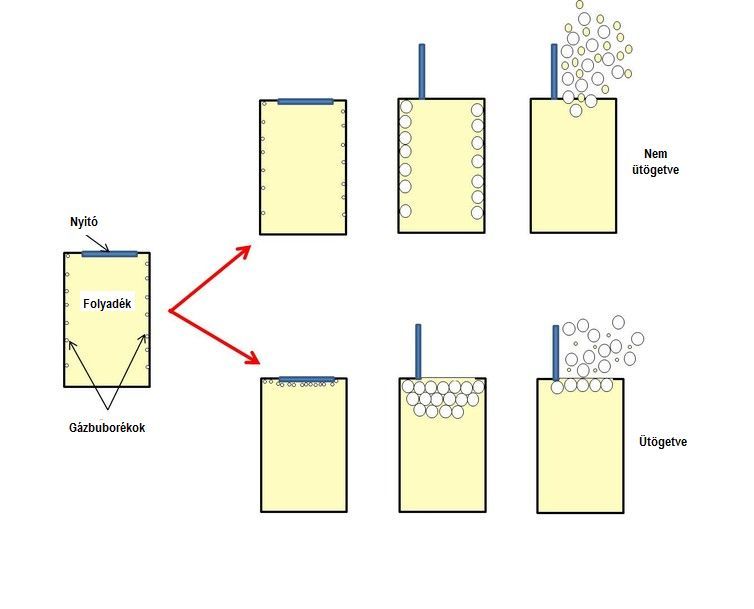
Az ütögetés hatására elválhat a faltól az odatapadt buborékok egy része, és ezek még a nyitás előtt a felszínre emelkednek. A dobozt kinyitva a buborékok kitágulnak, és azok, amelyek mélyebben voltak a folyadékban hosszabb távot tesznek meg, mint a felszín közelében lévők. Ezért az előbbieknek több italt kell „félrelökniük” az útból, és ezért valószínűleg több folyadékot löknek ki a dobozból.
A megütögetett dobozban kevesebb ilyen mélyebben lévő buborék van, ezért kevesebb folyadék mozdul el (és spriccel ki), mint a nem ütögetett doboz esetében.
A doboz oldalának ütögetése is hasonló hatású, de a tapasztalatok szerint kevésbé hatékony.
A buborékok természetesen a doboz erőteljes rázogatásakor is leválnak a falról, de ez a módszer több turbulenciát hoz létre, ami növeli a rendszer energiáját, ezért több buborék lesz az italban, és hevesebb spriccelés nyitáskor.
A spriccelés meleg italoknál is hevesebb, mint a hűtötteknél, mert a gázok oldhatósága a hőmérséklet emelkedésével csökken.












