Hegek nélküli szép bőrt ígér a forradalmi sebgyógyító módszer
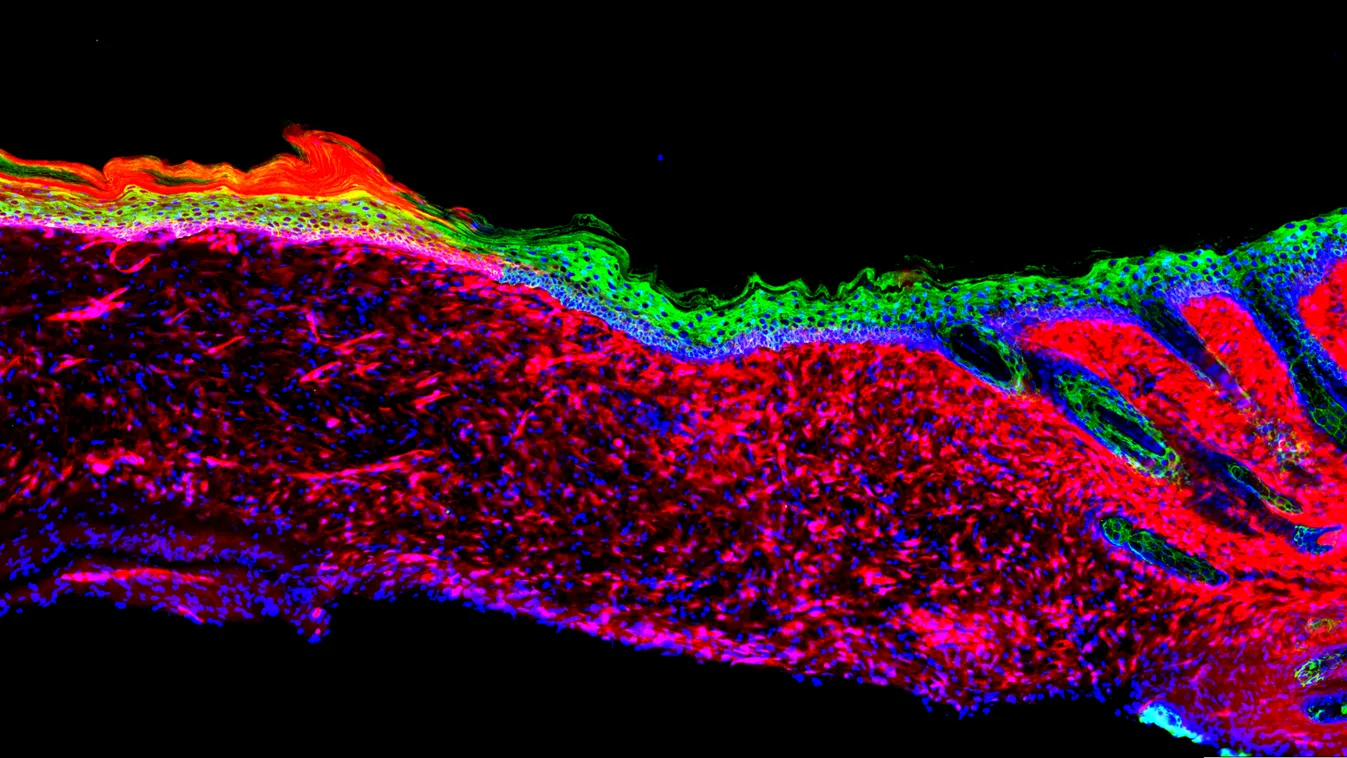

A nagyobb méretű sebeket – különböző okok miatt kialakult fekélyeket, égési sérüléseket – eddig csak plasztikai műtétekkel, bőrátültetésekkel tudták valamelyest helyrehozni. Amennyiben a károsodás túlságosan nagynak bizonyul, az orvosoknak nem áll mindig megfelelő mennyiségű átültethető szövet a rendelkezésére. Ilyen esetekben a pótlást izolált bőr-őssejtek laboratóriumi tenyésztésével tudják megoldani. Az eljárás bár működőképes, mégsem tökéletes.
Egyrészt míg visszaültethetővé válik a bőrszövet, elég sok időnek kell eltelnie, ami együtt jár a páciens életének kockáztatásával, másrészt drága procedúra, aminek végén hegek maradhatnak vissza.
Szintén nagy gond, hogy az öregedéssel a sebgyógyulás egyre nehézkesebbé válik. A bőr gyógyulási képességének romlása miatt még az apróbb sérülések is könnyen nehezen rendbejövő, komoly fájdalommal járó fekélyekké válhatnak.
Egy új kutatás sokkal effektívebb lehetőséget kínál a páciensek számára, mint a bőrtranszplantáció. A kaliforniai Salk Intézet (angolul Salk Institute for Biological Studies) munkatársai olyan technikát dolgoztak ki, amellyel a seb alapján található sejteket új bőrsejtekké transzformálják. A kísérletet egyelőre csak egereken végezték el, de az eddigi eredmények mindenképpen biztatóak.
A kutatók rájöttek, hogy a sebek begyógyításához vezető kulcslépést a keratinociták sérülésbe való ültetése jelenti. A keratinocita egyfajta őssejtekre hajazó sejt, prekurzorként szolgál a különböző típusú bőrsejtek számára. A felismerés során azonban egy újabb akadály merült fel; a nagyobb, több bőrréteg megsemmisülésével járó sérüléseknél nem marad bazális (alapi) keratinocita, és ha be is indul a gyógyulási folyamat, a helyben többszöröződő sejtek csak a nyílt seb zárására, gyulladás képzésére összpontosítanak, nem az egészséges bőrszövet újraépítésére.
A szakemberek ezért azt találták, a legjobb megoldás, ha a sejteket közvetlenül a sebesülés helyén, az élő szervezeten belül bazális keratinocitákká alakítják.
Valójában úgy hozunk létre bőrt, hogy közben nincs kéznél bőr, amiből ki tudnánk indulni"
– fogalmazott a kiadott sajtóközleményben Masakazu Kurita, a Salk Intézet egyik munkatársa.
Az alkalmazott módszert a Nature magazinban megjelent tanulmány rangidős szerzője, Juan Carlos Izpisua Belmonte mutatta be az Origónak.
A tanulmányban szereplő technikát a szakirodalom közvetlen újraprogramozásnak nevezi. Lényege, hogy egy adott sejttípust egy másikká alakítunk át úgy, hogy a célsejtben megváltoztatjuk a génkifejeződést
(szaknyelven génexpressziót – a szerk.). Ehhez vírusokat veszünk igénybe" – magyarázta Belmonte.
Első lépésként 80 „újraprogramozási faktor" (fehérjék és RNS-molekulák) közül kellett szelektálni. A cél olyanfajta faktorkombinációk megalkotása volt, amelyekkel a sejteket a leghatékonyabban lehet keratinocitákká változtatni.

Kétségtelenül ez bizonyult a legnagyobb kihívásnak.
Célunk olyan sejtek létrehozása volt a sebben, amik epiteliális szövetté alakíthatók, és hordozzák a bőr külső rétegének jellegzetességeit, illetve funkcióit.
Legjobb tudomásunk szerint hasonló jellegű kísérlettel még nem próbálkozott senki, továbbá az is kétséges volt, hogy a tökéletes kombinációk évekig tartó keresgélése során rálelünk-e a leginkább megfelelő összeállításra"
– mondta Belmonte.
A feladatra végül négy faktor együttese bizonyult alkalmasnak, a kutatók őket csomagolták vírusokba, és juttatták az egerek hátán indukált fekélyekbe. A „kórokozók" ezt követően sikeresen megfertőzték a sebben található, nem hámszöveti eredetű sejteket. Az infekció hatására a sejtekben végbemenő génkifejeződés megváltozott, lehetővé téve hámsejtekké való átprogramozásukat. Az újonnan létrejövő epiteliális sejtek már ki tudták alakítani azt a hámszövetet, aminek léte a seb teljes befedéséhez és gyógyulásához elengedhetetlen.
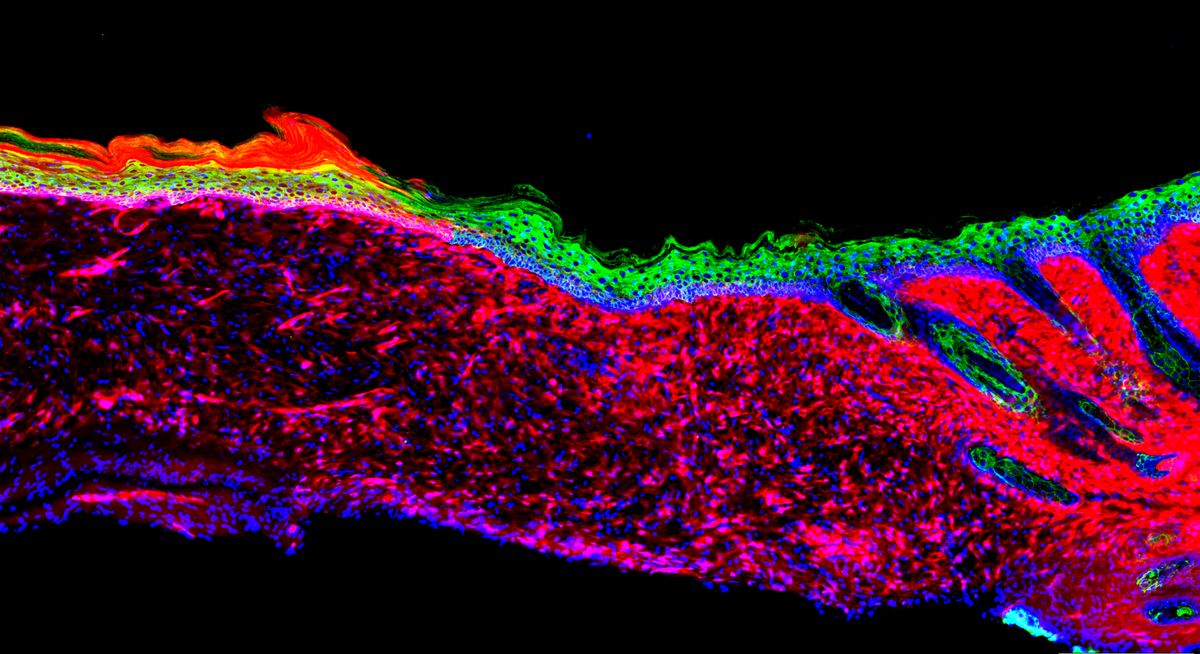
A végeredmény magáért beszél: a fekéllyel kezelt egereken 18 nap alatt kifejlődött az egészséges hámszövet. Idővel a hámképződmény kiterjedtté vált, összekötötte a környező bőrszöveteket. A folyamat még nagyobb sebesüléseknél is látványosnak számított.
Három-hat hónap múlva a létrehozott sejtek tökéletesen úgy viselkedtek, akár az egészséges bőrsejtek, az azonosságot genetikai és molekuláris vizsgálatok igazolták.
Belmonte hangsúlyozta, mielőtt a technikát klinikailag is alkalmaznák, további finomhangolásokra van szükség. Az egyik ilyen az újraprogramozás eredményesebbé tétele, valamint az esetleges kockázatok kiszűrése.
Mivel a vírusok megkerülhetetlen szereplői a történetnek, a kutatóknak ki kell derítenie, a módszer növeli-e rákos megbetegedés kialakulásának rizikóját.
Habár a tanulmányban nem írtak efféle veszélyről, mindenképpen hosszabb távú megfigyelésre lesz szükség, hogy lenullázzák a tumorok megjelenésének esélyét.
Belmonte szerint amennyiben a fentiek megvalósulnak, úgy az új metódus sikeresen kiválthatja a bőrátültetéseket, megnyitva a kaput a nagyobb sebek nyom nélküli gyógyítása előtt. Az sem kizárt, hogy más szervek, szövetek károsodásának helyrehozásában is alkalmazhatóvá válik az eljárásmód.












