



A hasnyálmirigyrák a különösen agresszív és nehezen kezelhető rosszindulatú daganatok közé tartozik, nem utolsó sorban azért, mert gyakran ellenálló a kemoterápiával szemben. Most a Stanford Egyetem kutatói kiderítették, hogy ez a terápiarezisztencia összefügg a daganatsejteket körülvevő kötőszövet fizikai keménységével és e szövet sejtközötti állományának kémiai összetételével. A Nature Materials anyagtudományi szakfolyóiratban publikált közlemény rámutat, hogy a terápiával szembeni ellenállás legyőzhető, és a szerzők lehetséges új célpontokat jelölnek ki a jövőbeni hasnyálmirigyrák-terápiák számára.
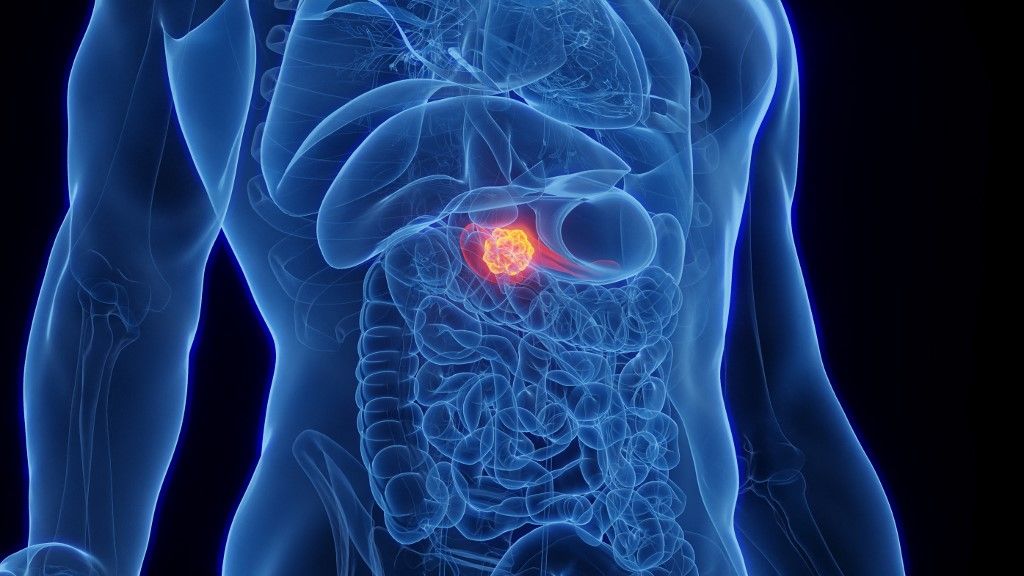
Fotó: Science Photo Library via AFP
Azt találtuk, hogy a merevebb szöveti környezet a hasnyálmirigyrák-sejteket ellenállóvá teszi a kemoterápiával szemben, míg a lágyabb szövetben a daganatsejtek jobban reagáltak ugyanarra a kezelésre
– fejtette ki Sarah Heilshorn, a Stanford anyagtudományi mérnöke és a cikk rangidős szerzője. – Eredményeink a hasnyálmirigyrák kezelésében komoly orvosi kihívást jelentő kemorezisztencia leküzdésének ígéretes új irányvonalát jelölik ki.
A hasnyálmirigyrák gyógyítása - ez lehet a megoldás?
A kutatók az ún. duktális hasnyálmirigyrákra összpontosítottak. Ez a hasnyálmirigy leggyakoribb, az esetek mintegy 90%-át kitevő formája, amely a mirigy kivezetőcsöveit bélelő hámszövetből indul ki. Ezekről a daganatokról ismeretes, hogy a sejtközötti állományuk, más néven extracelluláris mátrixuk – a sejtek közeit kitöltő, fehérjékből és cukrokból álló hálózatuk – feltűnően tömör és merev.
A tudósok régóta sejtik, hogy ez a tömör sejtközötti állomány fizikai gátként akadályozza a kemoterápiás szereknek a ráksejtekhez való hozzáférését, de azok a kezelési próbálkozások, amelyek ezt az akadályt próbálták leküzdeni, embereken nem bizonyultak sikeresnek.
Heilshorn és doktorandusz hallgatója, Bauer LeSavage, aki a cikk vezető szerzője, egy új rendszer kidolgozását tűzték ki célul a sejtközötti állományt érintő változások tanulmányozására és e változások ráksejtekre gyakorolt hatásának jobb megértésére. Olyan háromdimenziós anyagokat terveztek, amelyek egyfelől a hasnyálmirigyrák, másfelől az ép hasnyálmirigy szövetének biokémiai és mechanikai tulajdonságait imitálják, és ezekben az anyagokban tenyésztették a hasnyálmirigyrákos páciensekből származó daganatsejteket. A daganatos mintákat Calvin Kuo professzortól, a Stanford orvosi fakultásának tanárától szerezték.
Olyan, magunk kialakította mátrixokat terveztünk, amelyek lehetővé tették annak az elképzelésnek az ellenőrzését, miszerint a rákos sejtek reagálnak az őket körülvevő mátrix kémiai jelzéseire és mechanikai sajátságaira
– ismertette Heilshorn.
Fotó: Science Photo Library via AFP
Érzékennyé tennék a hasnyálmirigyrákot a kemoterápiára
Új kísérleti rendszerük segítségével a kutatók fajlagos módon aktiválták a daganatsejtek bizonyos fajta sejtfelszíni receptorait, és különböző módokon változtatgatták a maguk tervezte 3D mátrix kémiai és fizikai jellemzőit. Arra jutottak, hogy a hasnyálmirigyráknak két dolog kell ahhoz, hogy kemorezisztenssé váljon:
- fizikailag tömör, merev extracelluláris mátrix,
- illetve nagy mennyiségű hialuronsav.
Ez utóbbi egy jól ismert mátrixalkotó poliszacharid, amely merevvé teszi a sejtközötti állományt, és a CD44 nevű sejtfelszíni receptoron keresztül hat kölcsön a sejtekkel.
A merev, magas hialuronsavtartalmú mátrixba ültetett hasnyálmirigyrák-sejtek eleinte reagáltak a kemoterápiára, ám bizonyos idő után e körülmények hatására terápiarezisztenssé váltak: olyan fehérjéket gyártottak és helyeztek ki a sejtfelszínre, amelyek azelőtt kipumpálják a sejtből a kemoterápiás szereket, mielőtt azok hatni tudnának. A kutatók ugyanakkor azt is bizonyították, hogy ez a folyamat visszafordítható, akár úgy, hogy a sejteket lágyabb mátrixba telepítik át (még akkor is, ha annak hialuronsavtartalma magas marad), vagy úgy, ha blokkolják a CD44 hialuronsav-receptort (akkor is, ha a mátrix merevsége nem változik).
Vissza tudjuk billenteni a sejteket egy olyan állapotba, amelyben érzékenyek a kemoterápiára
– hangsúlyozta Heilshorn. – Ez azt vetíti előre, hogy ha a CD44 receptor által közvetített keménység-jelzést blokkolni tudjuk, a hasnyálmirigyrákos páciensek daganatai a normális kemoterápiás szerekkel újra kezelhetővé válhatnak.
A felfedezés, hogy a hasnyálmirigyrák-sejtek a CD44 receptoron keresztül kölcsönhatnak a merev extracelluláris mátrixszal, meglepetésként érte a kutatókat – mondta el Heilshorn. Más daganatok viselkedését is befolyásolják az extracelluláris mátrix mechanikai sajátságai, ám ezeket a jelzéseket jellemzően a sejtfelszíni receptorok egy másik osztálya, az ún. integrinek közvetítik.
„Rámutattunk, hogy a mi mátrixainkba ültetett hasnyálmirigyrák-sejtek igazából egyáltalán nem is az integrin-receptoraikat használják" – szögezte le a kutatónő.
Ez lényeges, mert ha olyan gyógyszereket akarunk tervezni, amelyek helyreállítják a páciensek daganatainak kemoterápia iránti érzékenységét, tudnunk kell, hogy pontosan melyik biológiai útvonalba kell beavatkoznunk.
Fotó: Science Photo Library via AFP
Mi a következő lépés?
Heilshorn és munkatársai most tovább vizsgálják a CD44 receptort, illetve az eseményeknek azt a láncolatát, amelyet a receptor aktiválása előidéz a daganatos sejtekben. Minél inkább felderítik a kemorezisztencia hátterében álló biológiai mechanizmusokat, annál könnyebb lesz a gyógyszertervezőknek kitalálniuk, miként nyúljanak bele ebbe a folyamatba.
A kutatók emellett továbbfejlesztik a sejtkultúrás modelljüket azzal, hogy további sejttípusokat adnak hozzá, amivel jobban utánozzák a daganatsejtek környezetét, és a mátrix merevségén kívül annak egyéb mechanikai tulajdonságait is megpróbálják módszeresen módosítani. Amellett, hogy munkájukkal új utat nyitnak a hasnyálmirigyrák kemorezisztenciájának megtörésében, a tudósok azt is remélik, hogy kutatásuk rávilágít az extracelluláris mátrixnak a daganat előrehaladásában betöltött szerepére, és hangsúlyozza a minél valósághűbb laboratóriumi modellek fontosságát.
„Amikor kemoterápiákat tervezünk, a sejttenyészeteinket olyan mátrixban kell fenntartanunk, amely a valódi páciensekéhez hasonlít" – emelte ki Heilshorn. – Ez ugyanis számít. A sejtek attól függően reagálnak így vagy úgy a gyógyszerekre, hogy milyen az őket körülvevő mátrix.


Itt az újabb ukrán támadás a békepárti Magyarország ellen

Magyar Péter vagy hazudik, vagy nőnek gondolja magát

Kitálalt az egyik anyuka: zokogva mentek haza a gyerekek Tóth Gabi táborából

Elbúcsúzott Liverpooltól, nagy útra indult Szoboszlai Dominik

Köpni-nyelni nem tudnak a rajongók: újra együtt van Curtis és ex felesége, Krisztike

Fordítva sült el Josep Borrell szimbolikus büntetése

Alig keres rajta, mégis ragaszkodik ehhez az olcsó menühöz a McDonald's

Lila, fehér, fekete: bemutatta új szerelését az Újpest – Videó

A többség nem támogatja az uinós külügyi biztos Magyarország ellenes tervét

Újabb szupertankokat kapott a Magyar Honvédség - képek

Az utcán, egy piros lámpánál kiabált egymással Győzike és L.L. Junior - videó


